Proktologie – Teil 1: Diagnostik
D. Wilhelm, L. Calavrezos
Chirurgische Klinik und Poliklinik, Klinikum rechts der Isar, Technische Universität München
Während die Proktologie als therapeutische Disziplin primär dem Gebiet der Viszeralchirurgie zuzuordnen ist, betrifft die Diagnostik proktologischer Erkrankungen hingegen jeden endoskopisch tätigen Arzt, sodass entsprechende grundlegende Kenntnisse vorhanden und eine sichere Beurteilung der häufigsten Krankheitsbilder gewährleistet sein müssen. Viele proktologische Befunde können sozusagen als Nebenprodukt einer Routinekoloskopie erhoben werden. Durch den routinemäßigen Einsatz der flexiblen Endoskopie bleiben häufig jedoch relevante Befunde verborgen, da diese erst mit der starren Endoskopie suffizient beurteilt werden können.
Diese mehrteilige Abhandlung über die Proktologie ist bemüht, die notwendigen proktologischen Kenntnisse zu vermitteln, beschränkt sich dabei aber auf die häufigsten Erkrankungsbilder. Im ersten Abschnitt sollen zunächst die Grundtechniken der proktologischen Untersuchung erläutert werden, die, wie bei jedem anderen Krankheitsbild auch, die Basis für eine erfolgreiche Behandlung darstellen.
Die proktologische Basisdiagnostik beinhaltet die ausführliche Anamnese, welche von der klinischen und apparativen Diagnostik gefolgt ist. Letztere umfassen die digital-rektale Untersuchung und die Prokto- und Rektoskopie. Zusätzliche Untersuchungen sind hingegen speziellen Fragestellungen vorbehalten und werden bei den betreffenden Krankheitsbildern erörtert (Abb. 1).
Die ausführliche proktologische Anamnese ist essentiell für ein vertrauensvolles Arzt-Patienten Verhältnis, stellt sogleich aber auch die wichtigste Säule der Diagnostik dar.
ANAMNESE
Viele proktologische Erkrankungen weisen eine typische Klinik auf, die mit der Anamnese erfasst werden kann und die Diagnosestellung wesentlich erleichtert. So betreffen schmerzhafte Erkrankungen, insbesondere wenn sie akut einsetzen, häufig das hochsensible Anoderm und die Diagnose einer Analfissur ist naheliegend, wenn Schmerzen erstmalig nach der Defäkation auftreten und einen intensiv-schneidenden Charakter aufweisen. Neben der freien Schilderung von Beschwerden durch den Patienten sollte die Anamnese verschiedene Symptomkomplexe gezielt abfragen. Dabei sind folgende Bereiche zu erfassen: Blutungen und Nässen, Schmerzen, Pruritus ani und Kontinenz- und Obstipationsproblematiken. Die ausführliche und gezielte Anamnese vermittelt dem Patienten zudem die ärztliche Kompetenz und schafft das Vertrauen, das für die spätere klinische Untersuchung entscheidend ist.
Folgende Aspekte sollten bei der Anamnese gezielt erfragt werden: Blutungen und Nässen, Schmerzen, Pruritus ani, sowie Kontinenz- und Obstipationsproblematiken
Blutung und Nässen
Blutungen sind für den Patienten immer beunruhigend, da sie mit Tumorerkrankungen assoziiert und in ihrer Intensität in der Regel überschätzt werden. Bei Blutungen ist es entscheidend zwischen akuten Blutungen (typisch für perianale Thrombosen, Fissuren, Divertikel und Hämorrhoiden) und chronischen Blutungen zu unterscheiden (entzündliche und neoplastische Erkrankungen). Überlappungen zwischen den Blutungsformen sind jedoch häufig, was entsprechend berücksichtigt werden muss. Helles Blut findet sich typisch bei Hämorrhoidal- und fissuralen Blutungen sowie bei Divertikelblutungen, wohingegen dunkles, koaguliertes Blut eher mit einer chronisch-entzündlichen oder neoplastischen Erkrankung korreliert. Unterschieden werden muss auch zwischen Blutauflagerungen auf dem Stuhl (Hämorrhoiden, Ulcus, Rektumkarzinom), blutdurchmischtem Stuhl (Colitis, Kolonkarzinom) und reinen peranalen Blutungen (Divertikelblutung, Hämorrhoiden). Da chronische Blutungen häufig als solche übersehen werden, sind klinische Zeichen der Anämie zu beachten, wie ein blasses Hautkolorit und blasse Skleren, aber auch eine mangelnde Belastbarkeit. Weniger beunruhigend, für den Patienten aber ebenso störend, ist das Nässen, welches Hinweis auf eine Inkontinenz sein kann oder bei dermatologischen Erkrankungen, wie dem Perianalekzem auftreten kann. Nässen ist meist mit einem Pruritus ani assoziiert (s.u.) und kann leicht über die benetzte Unterwäsche identifiziert werden. Die Frage nach verunreinigter Unterwäsche sollte daher zum Standardrepertoire der proktologischen Anamnese zählen. Bei höhergradigen Problematiken finden sich zudem Schleimabsonderungen, bei deren Auftreten immer nach einem Rektum- und Analprolaps und einer Inkontinenz gefragt werden muss, ggf. kann aber auch ein schleimbildendes Adenom vorliegen.
Die Verunreinigung der Unterwäsche ist ein sensibles Diagnostikum für Nässen, Inkontinenz, peranale Blutungen und den Pruritus ani.
Schmerz
Wie schon eingangs erwähnt ist der akut eingetretene Schmerz hinweisend auf eine Problematik des Anoderms und der Perianalregion, die zu den empfindlichsten Regionen des Körpers zählen, wohingegen Erkrankungen des Rektums meist keine oder nur geringe Schmerzen verursachen. Insbesondere für die Unterscheidung von Perianalvenenthrombosen und prolabierten Hämorrhoidalknoten, die proktologisch wenig erfahrenen Untersuchern häufig schwer fällt, ist dieser Aspekt von Bedeutung. So empfindet der Patient bei der Thrombose regelhaft einen intensiven Schmerz, der nur über Tage langsam abnimmt, wohingegen Hämorrhoiden nur bei Inkarzeration und ausgeprägten Thrombosierungen entsprechende Schmerzen bereiten. Stechende Schmerzen sind weiterhin typisch für den Herpes genitalis. Den am stärksten ausgeprägten Schmerz fühlen Patienten hingegen bei Fissuren, wobei dieser mit jeder Defäkation erneut zunimmt und zu der charakteristischen Anspannung des Sphinkterapparates führt. Ein zeitlicher Bezug des Schmerzes zur Defäkation ist daher bedeutend, sowohl was das initiale Ereignis anbetrifft, aber auch den weiteren Verlauf. Chronisch zunehmende Schmerzen, die dumpf und diffus wahrgenommen werden (protopathischer Schmerz), finden sich hingegen bei Abszessen und Fisteln und bei anderen entzündlichen Erkrankungen, aber auch beim Analkarzinom. Das Rektumkarzinom ist hingegen meist asymptomatisch, genauso wie zahlreiche dermatologische Erkrankungen.
Pruritus ani
Perineales Jucken wird häufig in Verbindung mit einer Parasitose gebracht (z.B. Wurmeier von Enterobius vermicularis), allerdings handelt es sich beim Pruritus meist um ein unspezifisches Symptom welches auf eine Überfeuchtung der Perianalregion hinweist und auf einen übermäßigen Kontakt mit reizenden Stoffen. Diese können aus dem Stuhl stammen (u.a. bei überhöhtem Konsum von Kaffee, Zitrusfrüchten und Schokolade) und damit einen Hinweis auf eine okkulte Inkontinenz (Fisteln, Hämorrhoiden) geben oder von außen zugeführt worden sein, wie etwa durch Kosmetika bei übermäßigen Einsatz von feuchtem Toilettenpapier und Seifen oder über die Kleidung. Da viele Patienten den Juckreiz durch eine übertriebene Analhygiene behandeln, entsteht hierdurch nicht selten ein circulus vitiosus über den die Patienten aufgeklärt werden müssen. Aber auch dermatologische Erkrankungen, wie das Perianalekzem, die Psoriasis, die Streptokokkendermatitis und Mykosen gehen häufig mit einem Pruritus einher. Da Patienten nicht selten einen perinealen Juckreiz verschweigen ist bei der klinischen Untersuchung auf sekundäre Zeichen, wie etwa Kratzspuren, zu achten.
Inkontinenz und Obstipation
Während die Inkontinenz primär ein Problem des älteren Patienten darstellt, sind Obstipations-beschwerden häufig bereits im mittleren und auch jungen Alter zu diagnostizieren. Inkontinenzsymptome werden häufig erst im fortgeschrittenem Stadium erwähnt (Grad III Inkontinenz für festen Stuhl), so dass nach leichten Formen (Feinkontinenzstörung, Grad I: Inkontinenz für Gase, Grad II: Inkontinenz für flüssigen Stuhl) gezielt gefragt werden muss. Hierbei sollte zeitgleich auch die Stuhlkonsistenz erfasst werden, da flüssige Stühle bei gestörter Sensibilität des Anorektums nicht perzeptiert und damit nicht kontrolliert werden können. Neben dem Grad der Inkontinenz wird nach der Häufigkeit des Auftretens, passiver und Dranginkontinenz sowie dem Stuhlschmieren, welches typisch für das Vorliegen einer Rektozele ist differenziert. Alle genannten Parameter geben Aufschluss über Schwere und mögliche Ätiologie der Inkontinenz und sollten idealerweise in Form eines standardisierten Fragenbogens erfasst werden, der zudem eine objektive Beurteilung im Verlauf einer Behandlung ermöglicht. Häufig eingesetzte Scoringssysteme sind der Wexner Score (Cleveland Clinic Florida Fecal Incontinence Score) und der Williams Score.
Auch für die Obstipation ist die Bestimmung der Stuhlkonsistenz relevant sowie die systematische Erfassung möglicher konditionierender Medikamente (z.B. bei M. Parkinson). Neben der Erfassung der Stuhlfrequenz rücken in letzter Zeit zunehmend auch assoziierte Beschwerden in den Vordergrund, wie im Rahmen der Rom Klassifikation umgesetzt. Idealerweise wird auch bei der Obstipation ein Bewertungssystem eingesetzt (ODS-Score nach Altomare oder Longo, oder der Cleveland Clinic Obstipation Score), welche unter anderem folgende Parameter erfassen: das Ausmaß der Stuhlentleerung und die Notwendigkeit der Unterstützung derselben, die Häufigkeit des Toilettengangs und die verbrachte Zeit auf der Toilette sowie assoziierte Beschwerden. Ein häufiger Toilettengang kann hierbei durchaus mit einer Obstipation zusammenhängen, vor allem wenn die Stuhlentleerung frustran oder inkomplett ist, charakteristischerweise bei Vorliegen einer Defäkationsstörungen (ODS=Obstruktives-Defäkations-Syndrom). Eine geringe Stuhlfrequenz findet sich hingegen häufiger bei Transportstörungen, wobei diese auch Folge einer Defäkationsproblematik sein können. Zudem sollte der Einsatz von Laxantien geklärt werden. Sowohl für die Inkontinenz, als auch die Obstipation sind vorrangegangene Operationen von Bedeutung (insbesondere proktologischer Art) sowie die Anzahl und der Verlauf von Geburten.
Bei der Obstipation treten begleitende Beschwerden und eine Unterstützung bei der Stuhlentleerung zunehmend in den Vordergrund der Diagnostik gegenüber der alleinigen Stuhlfrequenz, die bislang den entscheidenden Parameter darstellte.
KLINISCHE UNTERSUCHUNG
Die klinische Untersuchung unterscheidet die Inspektion und die digital-rektale Untersuchung, beides obligate Bestandteile der proktologischen Untersuchung. Die klinische Untersuchung stellt die zweite Säule der proktologischen Diagnostik dar. Für die suffiziente Beurteilung und Identifikation sind die Kenntnis des Normalbefundes und der anatomischen Gegebenheiten von Relevanz, sodass hierauf zunächst eingegangen werden soll.
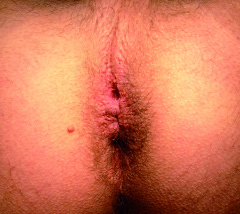
Der Anus grenzt sich aufgrund seiner feinen, radiären Fältelung gegenüber der umgebenden Perianalregion ab und weist auch ein anderes Kolorit auf, welche rosig bis bläulich imponieren kann. Der Anus sollte eine symmetrische Form aufweisen und kann je nach Patient eher flach oder trichterförmig imponieren. Der Anus sollte auch beim entspannten Patienten einen Grundtonus und Schluss aufweisen. Das epidermale Plattenepithel ist matt und allenfalls gegenüber der Perianalregion diskret reflektierend, muss aber vom glänzend-mukosalen Überzug des Rektums unterschieden werden, welcher beim Rektumprolaps sichtbar wird. Fistelöffnungen sollten ebenso fehlen wie eine diffuse (Perianalekzem) oder lokalisierte (Abszess) Rötung der Perianalregion. Der Anus setzt sich nach dorsal in die Rima ani und nach ventral in die Raphe des Skrotums fort (Abb. 2).
Der Anus ist zu Beginn der Untersuchung sorgfältig zu inspizieren, wobei der Patient hierfür eine für ihn angenehme Position einnehmen sollte. Dafür eignet sich in der Regel die Linksseitenlage oder, wenn verfügbar, die Steinschnittlagerung. Alle Auffälligkeiten sind mit Angabe der Position zu dokumentieren, wobei sich die Einteilung der Analregion analog zum Ziffernblatt einer Uhr bewährt hat. Hierbei entspricht die ventrale, der Symphyse zugewandte Seite des Anus der 12 und die zum Sakrum hin gelegene der 6 (entsprechend der Lage in Steinschnittlagerung, SSL). Die Untersuchung ist mit der notwendigen Sorgfalt und Diskretion vorzunehmen und sollte für den Patienten verständlich kommentiert werden (Abb. 3).
Bei der Inspektion der Analregion müssen alle Auffälligkeiten sorgfältig dokumentiert und in ihrer Lage beschrieben werden. Die Unterteilung des Anus analog dem Ziffernblatt einer Uhr hat sich hierfür bewährt.
Eingangs erfolgt die Inspektion der Analregion, wozu ggf. die Gesäßhälften auseinander gehalten werden müssen. Viele Erkrankungen können bereits hierbei diagnostiziert werden, etwa Abszesse, Condylomata, der Rektumprolaps oder die Perianalvenenthrombose. Marisken hingegen weisen in der Regel nur einen geringen Krankheitswert auf. Der After sollte einen regelhaften Schluss zeigen, ohne Zeichen der Inkontinenz, welche bei Nachweis von Stuhlreste oder Rötungen der Perianalregi-on (als Hinweis auf eine Feinkontinenzstörung) vermutet werden können. Dermatologische Erkrankungen, wie das Analekzem, die Mykose, das Condylom und neoplastische Veränderungen des Anoderms (M. Bowen) stellen häufig eine Blickdiagnose dar. Von besonderem Interesse sind Knotenbildungen jeglicher Art und das Vorhandensein von Narben als Hinweis auf eine vorangegangene Operation. Neben der alleinigen Inspektion sollte der Patient zum Pressen und Anspannen des Schließmuskels aufgefordert werden, um eine grobe Funktionstestung des Schließmuskelapparates zu erhalten. Es ist wichtig hierbei auf einen ausreichend langen Pressakt zu achten, da leichte Formen des Rektumprolapses und von Hämorrhoiden ansonsten übersehen werden könnten. Erneut sei hierbei auf eine ausreichende Entspannung des Patienten hingewiesen. Beim Pressen muss der Beckenbodens tiefer treten und der Schließmuskel entspannen, in der Regel kommt es hierbei auch zu einem Hervortreten des Anoderms. Reziprok führt das Anspannen des Anus zu einem Höhertreten des Beckenbodens. Orientierende neurologische Basistests ergänzen die Inspektion. Beim sogenannten Anokutaneus-Reflex kommt es nach peranaler Reizung zu einer Sphinkterkontraktion. Zudem sollte die perianale Sensibilität seitengetrennt erfasst werden.
An die Inspektion schließt sich die digital-rektale Untersuchung an, welche nicht auf die alleinige Beurteilung des Analkanals beschränkt werden sollte, sondern auch die Beurteilung der Perianalregion beinhaltet (Knoten, Indurationen, Fluktuationen, Fistelstränge). Die digital-rektale Untersuchung sollte erst nach einer sorgfältigen Anamnese durchgeführt werden, da sich hieraus diagnoserelevante Informationen für die Untersuchung ergeben und das weitere Vorgehen beeinflusst werden könnte. Die digitale Austastung des Analkanals kann unter Umständen sensibler sein, als die optische Beurteilung mit dem Prokto-/Rektoskop, bzw. ist die diagnostische Qualität nach grober digitaler Lokalisation deutlich höher (Fisteln, Analpapille, Fissuren, Analkarzinom). Entsprechend kommt der digitalen Untersuchung ein besonderer Stellenwert zu.
Die obligate digitale-rektale Untersuchung ist vor allem im Analkanal eine hoch-sen-sible diagnostische Maßnahme.
Bei der digital-rektalen Untersuchung sollte darauf geachtet werden, sich ausreichend Zeit zu nehmen und entsprechend sorgfältig vorzugehen. Hierfür sollten die Perianalregion und der untersuchende Finger mit einer ausreichenden Menge anästhesierenden Gleitgels benetzt werden und der Finger sodann langsam in den Analkanal ein-geführt werden. Hierbei sollte der Patient zum Pressen und damit zum Entspannen des Sphinkters aufgefordert werden. Der physiologische Verlauf des Analkanals nach ventral sollte hierbei berücksichtigt werden. Konnte eine schmerzhafte Region vorab abgegrenzt werden (z.B. Analfissur die meist bei 6 Uhr lokalisiert ist), empfiehlt es sich den Finger zur Entlastung des betroffenen Bereichs exzentrisch einzuführen, bzw. kann eine suffiziente Untersuchung bei schmerzhaften Prozessen erst nach Sedierung des Patienten erfolgen. Neben der Beurteilung oberflächlicher Veränderungen des Analkanals sollte hier erneut der Sphinktertonus in Ruhe, beim Kneifen und während des Pressens evaluiert werden. Bei entsprechender Erfahrung kann der Finger eine aufwendige manometrische Untersuchung ersetzen. Beim Pressen ist insbesondere auf eine Erschlaffung des Sphinktertonus zu achten (anorektaler Reflex). Vor allem beim obstruktiven Defäkationssyndrom kommt der Untersuchung eine hohe Bedeutung zu. Die Kontinuität des Sphinkters und die Sphinkterlänge sollten ebenfalls in die Beurteilung einfließen. Insbesondere sphinkternahe Rektumtumore können bzgl. ihrer Lagebeziehung digital hervorragend beurteilt werden, wobei der Patient zur Abgrenzung des Sphinkters zum Anspannen desselben aufgefordert werden sollte. In der weiteren Untersuchung sollte die Rektumampulle in ihrer gesamten Zirkumferenz ausgetastet werden. Eventuell vorhandene Rektozelen und Intussuszeptionen können bereits digital erfasst werden. Hierbei ist auch auf mögliche Neoplasien und Indurationen zu achten, wobei nochmals darauf hingewiesen werden sollte, dass etwa ein Drittel der Rektumkarzinome digital-rektal getastet werden können. Hierbei sollte auch auf die Verschieblichkeit gegenüber der Umgebung/Darmwand geachtet werden (Mason Klassifikation). Durch bi-digitale Beurteilung der Perinanalregion zwischen Daumen und intraanalem Finger können tiefgelegene Abszesse und auch Fistelgänge identifiziert werden. Vor allem bei dumpfen, tiefen Schmerzen ist diese Untersuchung daher zu ergänzen. Andere Pathologien, wie Hämorrhoiden sind hingegen eher einer optischen-proktologischen Diagnostik zugänglich, können aber ggf. als weiches Polster gespürt werden. Das Abtasten der Prostata, bzw. der Zervix schließt die Untersuchung ab.
PROKTOSKOPIE/REKTOSKOPIE
Die proktologische Basisuntersuchung wird durch die Proktoskopie und Rektoskopie abgeschlossen, die routinemäßig erfolgen sollten, wobei beide Methoden eine jeweils gesonderte Indikation aufweisen; sie werden somit nicht komplementär eingesetzt. Die Bedeutung der starren Rektoskopie hat allerdings in den letzten Jahren abgenommen. Sie hat ihren Stellenwert nur noch in einzelnen Teilbereich beibehalten, etwa bei der Bemessung des Abstandes rektaler Tumoren zum Analrand oder bei Rektozelen und Intussuszeoptionen. Die Proktoskopie weist hingegen ein klares Alleinstellungsmerkmal gegenüber der flexiblen Endoskopie auf, der sie zur Beurteilung von Prozessen des Analkanals klar überlegen ist. Zudem ist der Aufbereitungsprozess der starren Instrumente deutlich günstiger, was bei der alleinigen Beurteilung analer Prozesse berücksichtigt werden muss. Beide Instrumente entsprechen einer Metallhülse mit Anschluss an eine Lichtquelle, welche der Illumination dient, wobei das Rektoskop deutlich länger (20-25cm) und gasdicht abschließbar ist. Mit dem Rektoskop kann bis in das distale Sigma eingespiegelt werden. Das Proktoskop ist hingegen offen und kürzer. Aufgrund der starren Auslegung gelingt es mit beiden Geräten die Schleimhaut des Analkanals aufzuspannen und suffizient zu beurteilen. Dadurch, dass beide Instrumente den Analkanal ohne Gaseinblasung offen halten, können insbesondere Hämorrhoiden gut beurteilt werden (Abb. 4).
Während die Bedeutung der Rektoskopie tendenziell abnimmt, stellt die Proktoskopie weiterhin eine unabdingliche Methode dar.
Proktoskopie
Eine spezielle Vorbereitung ist für Proktoskopie in der Regel nicht erforderlich, ggf. kann ein Klysma verabreicht werden. Wie oben erwähnt, sollte die Proktoskopie erst nach ausführlicher Anamnese und digitaler Untersuchung durchgeführt, eine Aufklärung sollte zudem und trotz der Risikoarmut der Untersuchung vorliegen. Für die Untersuchung sollte der Patient erneute eine entspannte Lage einnehmen, etwa die Linksseitenlage oder die Steinschnittlage. Das Proktoskop wird vorsichtig und unter begleitender Erläuterung in den After eingeführt, wobei unterschiedliche Größen je nach anatomischer Gegebenheit eingesetzt werden können. Das Proktoskop besitzt einen internen Obturator, der bei zurückgezogener Lichtquelle von innen scheint und mit seiner konischen Spitze das Einführen des Proktoskop erleichtert. Hierzu wird es mit ausreichend Gleitmittel versehen und senkrecht zur Perinealregion mit Schubrichtung zum Nabel drehend eingeführt. Erneut hat es sich dabei bewährt, den Patienten zum Pressen aufzufordern, um eine Entspannung der Sphinkteren zu erwirken. Auch die zuvor erfolgte, rektal-digitale Untersuchung unterstützt den Einführungsvorgang, da hierdurch bereits eine geringe Dehnung und Anästhesierung des Analkanals erfolgt ist. Nach Passieren der Sphinkterregion (3-5 cm ab ano) muss das Prokto-/Rektoskop entsprechend dem anatomischen Verlauf des Rektums (anorektaler Winkel) nach sakral abgekippt werden. Bei der Intubation ist es von größter Bedeutung ausreichend Zeit zu verwenden und das genaue Vorgehen zu erläutern.
Auch sollte das Proktoskop handwarm erwärmt sein und nicht gegen Widerstand blind intubiert werden. Wie auch schon bei der digitalen Untersuchung erwähnt, kann es notwendig werden, den Patienten zu sedieren, etwa beim Vorliegen einer Fissur. Das Proktoskop sollte bis zum Anschlag eingeführt werden, um eine vollständige Beurteilung des Analkanals auch bei Vorliegen eines Trichteranus zu gewährleisten. Sodann wird der interne Obturator entfernt, die Kaltlichtquelle angeschlossen und das Proktoskop unter kreisenden Bewegungen, die einen Aufblick auf die gesamte Zirkumferenz erlauben, langsam zurückgezogen. Hierbei ist das Proktoskop aufgrund seiner Länge deutlich besser zu steuern, als das Rektoskop. Zudem ist die Lichtausbeute aufgrund der Kürze des Instruments überlegen. Dennoch kann es mitunter schwierig sein, diskrete Befunde zu exponieren, weswegen Lokalisationen, die in der digitalen Untersuchung auffällig waren, besonders aufmerksam beurteilt werden müssen. Darüber hinaus empfiehlt es sich, die Prädilektionsstellen proktologischer Erkrankungen (Kryptenregion, Hämorrhoidalkomplexe bei 3, 7 und 11 Uhr SSL, Fissuren bei 6 Uhr SSL etc.) gesondert zu beurteilen. Bezüglich der Lokalisation potentieller Fisteln sei auf die Goodsall´sche Regel verwiesen. Dabei müssen die internen Fistelöffnungen nicht zwingend in der Kryptenregion liegen, sondern können auch im distalen Rektum auftreten. Ggf. kann die Untersuchung durch den Einsatz von Sonden und Farbstofflösungen, die in äußere Fistelöffnungen eingebracht werden, unterstützt werden. Auch indirekte Zeichen, wie hypertrophe Analpapillen und Vorpostenfalten, als Zeichen für eine chronische Fissur, sollten beachtet werden. Situativ kann es von Vorteil sein den Analkanal unter Verwendung von Watteträgern oder Pinzetten zu exponieren.
Auf die Bedeutung von eitriger Sekretion und verdickten Krypten sei hingewiesen. Bevor das Proktoskop in den Analkanal zurückgezogen wird, sollte der Patient zum Pressen aufgefordert werden, um ggf. vorhandene Rektozelen oder einen inneren Rektumprolaps zu verifizieren. Auch auf Höhe des Hämorrhoidalkomplexes sollte der Patient erneut zum Pressen aufgefordert werden, um einen Hämorrhoidalprolaps beurteilen zu können. Die Beurteilung von Hämorrhoiden erfolgt hingegen in Ruhe ohne Provokation. Für die Gummibandligatur von Hämorrhoiden können entsprechende Instrumente einfach über das Proktoskop eingeführt werden, aber auch die Blutstillung und Unterspritzung kann einfach vorgenommen werden.
Das Proktoskop dient der Beurteilung des Analkanals, zur Diagnose und Behandlung von Hämorrhoiden und zur Abklärung von Fisteln und Fissuren.
Die Intubation des Rektoskops erfolgt analog und ebenfalls mit einliegendem Obturator. Das Rektoskop sollte jedoch nicht maximal eingeführt werden, sondern nach Passage des Analkanals der Obturator gegen die Lupenkappe getauscht werden. Diese verschließt das Rektoskop luftdicht, sodass die weitere Intubation unter Sicht vorgenommen werden kann. Das Vorführen des Endoskops bietet hierfür zudem die Möglichkeit der Luftinsufflation mit Ballon, wodurch das Rektum expandiert werden kann. Unter Sicht und unter Illumination mit dem angeschlossenen Lichtleiter kann das Rektoskop um das rektale Faltenrelief bis ins untere Sigma vorgeführt werden. Im Gegensatz zur Proktoskopie ist daher eine Vorbereitung mittels Klysma empfehlenswert. Insbesondere durch die mögliche Luftinsufflation eignet sich die Rektoskopie zur Diagnose von Rektozelen und rektalen Ulzera, aber auch entzündliche und neoplastische Veränderungen können hervorragend beurteilt und bioptisch gesichert werden. Hierfür dienen spezielle, lange Biopsiezangen. Auch eine Blutstillung durch Unterspritzung oder Koagulation ist rektoskopisch möglich. Gerade für die Therapie der häufig intensiven Blutungen im Rektum ist das Rektoskop hervorragend geeignet, da sich auch größere Koagel gut absaugen lassen und potente HF-Sonden aus der offenen Chirurgie nutzen lassen. Ebenso wie in der Proktoskopie lassen sich aber auch interessierende Areale unter Verwendung von Stiltupfern exponieren. Ein Nachteil der Proktoskopie und Rektoskopie liegt in der Befunddokumentation und –demonstration, die deutlich eingeschränkt sind, da konventionelle Proktoskope/Rektoskope nicht über eine Videoanbindung verfügen.
Die Rektoskopie dient der Beurteilung des Rektums und hier gelegener Tumoren, sowie bei Rektozelen und der rektalen Intussuszeption
Zusätzliche Untersuchungen
Diese proktologische Basisuntersuchung kann durch weitere Methoden ergänz werden, die jedoch speziellen Fragestellungen vorbehalten sind. Hierbei ist vor allem die Endosonografie zu nennen, die das Spektrum der Diagnostik auf tiefergelegene Schichten erweitert und trotz immer besser werdender MR-Technologie immer noch indiziert ist. Daneben kommen verschiedene radiologische Untersuchungen, wie die Defäkografie und die Passagezeit-Bestimmung zum Einsatz. Die anale Manometrie und Elektrophysiologie ist vor allem zur Abklärung der Inkontinenz und selten bei obstruktiven Störungen angezeigt.
Abbildung 1
Abbildung 2
Abbildung 3
Abbildung 4
Was Sie hierzu wissen müssen
Metaanalysen aus kleineren Studien seit Beginn der 2000er Jahre zeigten gleichwertige Ergebnisse zwischen offener und laparoskopischer Chirurgie beim Rektumkarzinom; die letzte veröffentlichte Metaanalyse in einem größeren Journal – wie so oft aus China (1) – schloss 6 randomisierte Studien mit 1033 Patienten ein, darunter auch eine von 2003 mit 28 Patienten (sic!) aus einer lokalen brasilianischen Zeitschrift der Universität von Sao Paolo (Rev Hosp Clin Fac Med Univ Sao Paolo), die die Autoren hoffentlich als Vollpublikation in Originalsprache gelesen haben. Die anderen Studien sind in englischsprachigen Journalen veröffentlicht, aber teilweise so klein (Fallzahl insgesamt 99-204), dass es schon eines genialen Statistikers bedarf, um hier andere als gigantische Unterschiede zu ermitteln. Die einzige vernünftige Studie, der CLASSIC trial (n=381) (2) zeigte keinen Unterschied im zirkumferentiellen Resektionsrand, aber eine etwas geringere (HR 0.72) 3-Jahres-Überlebensrate, allerdings ein identisches krankheitsfreies 3-Jahres-Überleben. Insgesamt sind die Ergebnisse der „Metaanalyse“ für beide Verfahren ausgeglichen, was die statistische Analyse betrifft, doch lassen die Zahlen der Hazard Ratios daran denken, dass die Fallzahl trotzdem nicht ausreichend ist (2). Und weil‘s so schön ist, haben dieselben Autoren 2014 nochmal in einem kleinen lokalen Journal nochmal eine Metaanalyse veröffentlicht, diesmal mit 16 Studien, die meisten hätten auch schon 2011 eingeschlossen werden können (3). Also Vorsicht mit Metaanalysen.
Im April diesen Jahres erschien eine große europäische Studie an 1044 Patienten (COLOR II-Studie), die gleichwertige onkologische Ergebnisse im 3-Jahresverlauf zwischen beiden Verfahren zeigte, was lokoregionale Rezidive, krankheitsfreies und Gesamtüberleben betraf. Die Fallzahl (aus 30 Kliniken über einen 4-Jahres-Zeitraum) ist also ähnlich hoch wie die der 6 in der o. g. Metaanalyse eingeschlossenen Studien; weit fortgeschrittene Tumoren (u. a. T4) waren allerdings ausgeschlossen, die Grenze lag bei 15 cm ab ano. Die Randomisierung betrug 2:1 für die Chirurgie; knapp 60% und etwa 1/3 hatten präpoperativ eine Strahlen- oder Chemotherapie. Follow-up-Daten nach 3 Jahren waren je nach Parameter in 74%-89% der Patienten vorhanden. Die Studie war auf Gleichheit bzw. non-inferiority berechnet (4). Nach 3 Jahren stellten sich die Ergebnisse wie folgt dar
| Laparoskopisch | Offen | Unterschied | |
|---|---|---|---|
| Lokoregionales Rezidiv | 5.0% | 5.0% | 0 |
| Krankheitsfreies Überleben | 74.8% | 70.8% | 4.0 n.s. |
| Gesamtüberleben | 86.7% | 83.6% | 3.1 n.s. |
In beiden Gruppen war der zirkumferentielle Resektionsrand in 10% nicht tumorfrei (definiert als 2 mm Abstand), auch die sonstigen Daten zur kompletten Resektion waren nahezu identisch.
Im Nachgang sind gerade in JAMA zwei kleinere randomisierte Studien aus den USA/Kanada (n=489) und Australien/Neuseeland (n=475) erschienen, die bei den onkologischen Parametern der beiden Operationen (kein Follow-up vorliegend) schlechtere Ergebnisse für die laparoskopische Variante erbrachten. Die US-Studie (5) aus 35 Kliniken präsentierte die Ergebnisse von 486 eingeschlossenen und 462 auswertbaren Patienten mit Rektumkarzinomen (bis 12 cm ab ano, kein T4) über 5 Jahre – also im Schnitt knapp 3 Patienten pro Zentrum und Jahr: Das bedeutet nicht, das hier Unerfahrene am Werk waren, sondern wie üblich im klinischen Alltag, die meisten Patienten aus Zeit- oder sonstigen organisatorischen Gründen nicht eingeschlossen wurden oder nicht zugestimmt haben (die infrage kommende Zahl wird nicht genannt). Außerdem schließen Zentren unterschiedlich gut ein und es ist auch nicht klar, ob alle Kliniken zum gleichen Zeitpunkt mit der Studie begonnen haben. Diese Patientenselektion, die man bei fast allen Multizenterstudien hinnehmen muss, kann aber grundsätzlich dazu führen, dass die Representativität der Daten für alle infrage kommenden Patienten zumindest ein Diskussionspunkt ist. Ähnlich ging die Studie aus Australien und Neuseeland vor (6), hier schlossen über viereinhalb Jahre 24 Zentren 475 Patienten ein (473 wurden ausgewertet). T4-Tumoren wurden auch hier geschlossen, das Rektum war hier wie in Europa 15 cm lang. Beide Studien hatten noch kein Follow-up, sodass Hauptoutcome-Parameter histopathologische Parameter waren: Es wurde derselbe Composite-Score aus distalem und zirkumferentiellen Resektionsrand (> 1 mm) sowie der Qualität der gesamten mesorektalen Exzision bei geblindeter Pathologie. Als vollständige Resektion wurde gewertet, wenn alle Endpunkte in Nordamerika vollständig oder nahezu (d. h. R0 bei Abstand von unter einem mm) und in Australien komplett erreicht wurden. Die Ergebnisse sahen dann wie folgt aus
| Composite Outcome | Laparoskopisch | Offen |
|---|---|---|
| USA/Kanada | 92.1% | 95.1% |
| Australien/Neuseeland | 82% | 89% |
Aufgrund der unterschiedlichen Definitionen lohnt sich – zumindest für den Chirurgen – aber doch ein Blick in die drei o. g. Einzelparameter, wenn man die 1 mm-Grenze in beiden Studien strikt einhält, komplette Resektionen waren zu verzeichnen wie folgt
| Zirkumfer. Resektionsrand | Laparoskopisch | Offen |
|---|---|---|
| USA/Kanada | 87.9% | 92.3% |
| Australien/Neuseeland | 65.8% | 75.3% |
| Europa | 90% | 90% |
| Distaler Resektionsrand | Laparoskopisch | Offen |
|---|---|---|
| USA/Kanada | 92.1% | 95.1% |
| Australien/Neuseeland | 98.3% | 98.2% |
| Komplette totale mesorektale Exzision |
Laparoskopisch | Offen |
|---|---|---|
| USA/Kanada | 92.1% | 95.1% |
| Australien/Neuseeland | 87% | 92% |
Hier zeigt sich, dass der distale Resektionsrand kein Problem war, wohl aber der zirkumferentielle, und dies v. a. in den USA (wenn auch in beiden Gruppen). Der Vergleich mit der europäischen Studie, wo nur der zirkumferentielle Resektionsrand berichtet wurde, zeigt die Unterschiede am deutlichsten.
Die widersprüchlichen Ergebnisse sind nicht ganz leicht zu interpretieren, die NEJM-Studie ist größer und hat onkologische Outcomes statt Surrogatparameter, das Follow-up fehlt. Liegt es an der chirurgischen Qualität? Diese wurde aber mit Minimalzahlen und einem begutachteten Video einer Prozedur vor Studienbeginn ziemlich gut festgelegt, trotzdem hatten die europäischen Gruppen vielleicht doch die höhere Expertise. Aber die Statistik ist für Laien schwer zu lesen, die Mittelwerte der Hauptoutcomeparameter (Composite Score s. o.) liegen bei beiden Studien im angenommenen Bereich der Non-Inferiority: Die Studien haben in der Methodik eine Spanne von 6% (Nordamerika) bzw. 8% (Australien) für Non-Inferiority angenommen. Im Composite Score erreicht Nordamerika Unterschiede von 3%, und Australien von 7%, also beide scheinbar im grünen Bereich, die p-Werte sind auch unter 0.05. Trotzdem muss man die Gesamtspanne nehmen: Hier liegt die Untergrenze der tatsächlichen Ergebnisspanne (lower bound, 95% Konfidenzintervall) in Nordamerika bei -10.8% (angenommen wurden 10%) und in Australien bei -12.4% (angenommen wurden 8%), also Ziel ganz knapp verfehlt. Wenn man allerdings tiefer in die statistische Beratung einsteigen muss, um Ergebnisse zu verstehen, kommen leichte Unwohlgefühle auf. Vielleicht sind beide Studien einfach nicht ausreichend gepowert? Letztlich bleibt aber die Kritik am Hauptparameter der Studie, der ein Surrogatparameter ist, und das Follow-up, kann, wie die Autoren selbst diskutieren, hier andere Aufschlüsse bringen – hoffentlich sind beide Studien hierfür gepowert. Mehr Geduld gegenüber dem Veröffentlichungsdrang wäre also manchmal hilfreich… Bis dahin bleibt aus unserer Sicht die NEJM-Studie die überlegene für unsere Evidenz und die Warnung, die laparoskopische Chirurgie zurückzustellen würden wir so nicht stehen lassen wollen. Eine Zentralisierung dieser Eingriffe und dadurch bessere Konzentration von Erfahrung ist aber sicher anzustreben.